Nieuw mechanisme van het antibioticum tetracycline gevonden
8 maart 2021
Het team van microbiologen werd geleid door Michaela Wenzel en Leendert Hamoen van de groep Bacterial Cell Biology. Voor hun lopende onderzoek waren zij bezig een techniek te verbeteren waarmee bacteriën beter te meten zijn voor elektronenmicroscopie. Om hun nieuwe techniek te testen, volgden ze de morfologische reactie van bacteriën behandeld met antibiotica. Verrassend genoeg deden ze daarbij een interessante ontdekking, en vonden ze een nieuw mechanisme in de werking van het bekende antibioticum tetracylcine.
Veelgebruikt antibioticum
Tetracyclines zijn een van de meest gebruikte antibioticumgroepen in zowel diergeneeskunde als humane geneeskunde. Tetracycline is effectief tegen een breed scala aan bacteriën. Tot dusver was bekend dat het werkingsmechanisme van tetracycline bacteriële groei en overleving verhinderen omdat het bacteriële ribosomen blokkeert. Ribosomen zijn onderdelen in een cel die ervoor zorgen dat eiwitten gemaakt worden. Deze ribosomen zijn in alle bacteriën aanwezig, en daarom bleek tetracycline succesvol tegen veel verschillende bacteriële infecties. Dit succes heeft echter een keerzijde, namelijk dat bacteriën resistent kunnen worden. Resistentie kan optreden tegen allerlei soorten antibiotica, dus ook tegen tetracycline.
Door precies te weten te komen welke mechanismen antibiotica gebruiken om bacteriegroei te blokkeren, is het mogelijk te achterhalen hoe bacteriën deze mechanismen omzeilen als ze resistent worden. Daarom is het belangrijk om fundamenteel onderzoek te doen naar hoe bacteriën groeien, en wat er gebeurt als ze worden blootgesteld aan antibiotica. Deze kennis draagt bij aan het voorkomen van resistentie, en hopelijk helpt het ook om aanwijzingen te vinden voor de ontdekking en ontwikkeling van nieuwe moleculen met antibiotische werking.
Nieuw protocol
Het doel van de studie was het optimaliseren van een techniek om bacteriën efficiënter te bestuderen via transmissie-elektronenmicroscopie (TEM). TEM is een microscopietechniek waarmee onderzoekers de morfologie en ultrastructuur van bacteriën en andere zeer kleine cellen in detail kunnen bestuderen. Hoewel de techniek al meer dan 60 jaar wordt gebruikt om bacteriën te bekijken, is de wijze waarop de bacteriën worden voorbereid gelijk gebleven. Wenzel en collega’s vonden dat de huidige techniek een belangrijke beperking heeft: dat er geen controle is op hoe de bacteriën georiënteerd zijn.
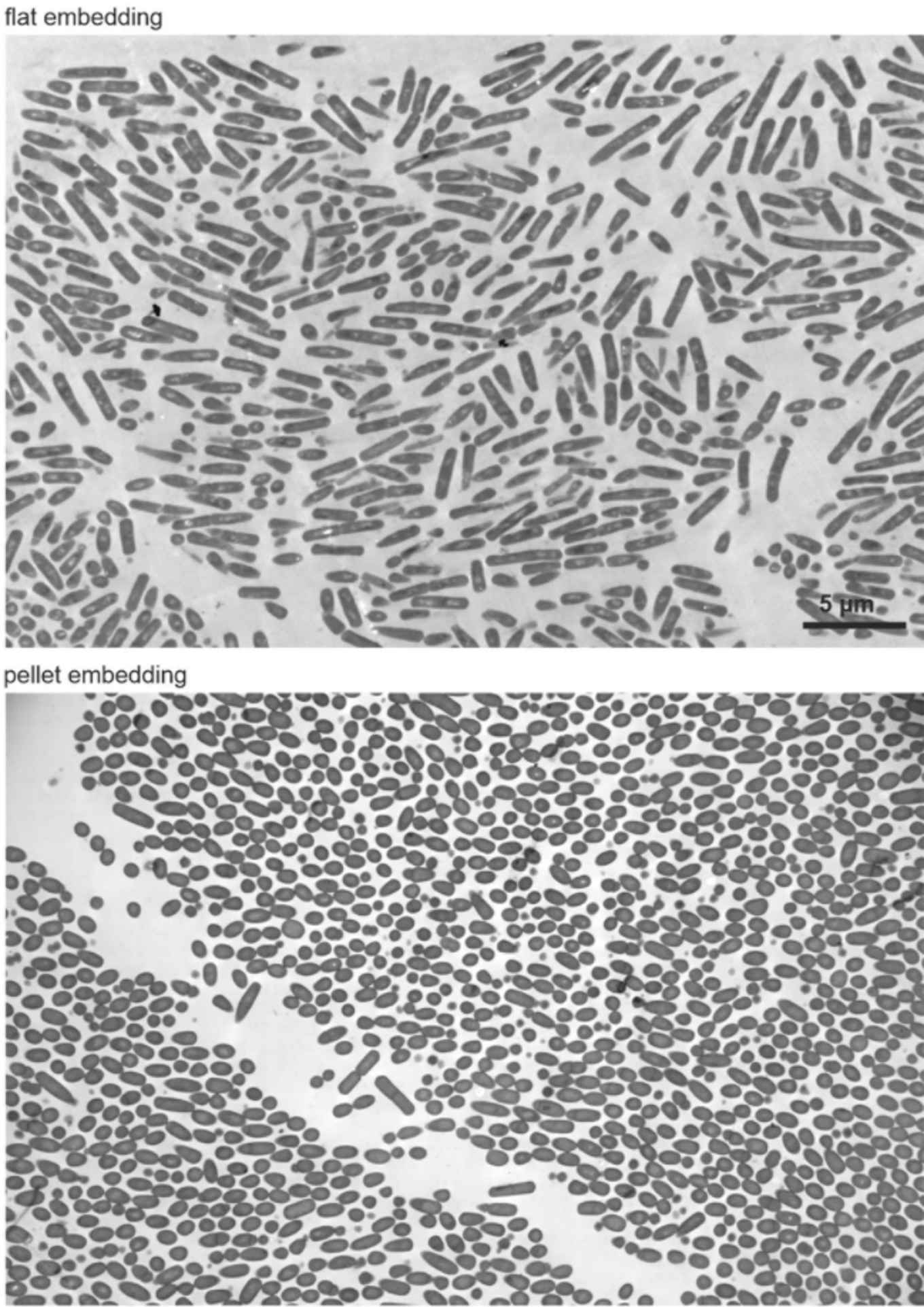
Bij het bestuderen van staafvormige bacteriën betekende dit dat ze veel tijd moesten besteden aan het zoeken naar bacteriën die op de juiste manier in de microscoop zichtbaar zijn, waarbij de hele lange zijde zichtbaar is. Ze optimaliseerden een protocol waarbij alle bacteriën op een plat oppervlak werden ingebed, zodat alle bacteriën in de juiste oriëntatie onder de microscoop komen te liggen. Dit zorgt voor een drastische verbetering van het aantal bacteriën dat per experiment kan worden afgebeeld, terwijl er veel minder bacteriën nodig zijn om een experiment in te zetten, en het veel minder tijd kost om grotere aantallen goed te kunnen meten.
Nieuw mechanisme
Om de nieuwe techniek te testen, gebruikten de onderzoekers deze om de reactie van de in het lab veelgebruikte bacteriestam Bacillus subtilis op tetracycline te bekijken via TEM. Daarbij maten ze vervormingen in het membraan van de bacteriën. Dit leek niet te komen door het blokkeren van ribosomen. Via een reeks experimenten doken ze vervolgens in de details wat er aan de hand was. De onderzoekers onderzochten de lokalisatie van drie verschillende eiwitten in het membraan van de bacteriën met hulp van een fluorescent label. Daarbij zagen ze dat de eiwitten op een verkeerde plaats kwamen te zitten in het membraan door tetracycline. Deze werking van tetracycline was nog niet eerder gevonden.
Resistentie tegen tetracycline ontstaat relatief langzaam, terwijl dit niet het geval is voor andere antibiotica die ook ribosomen blokkeren. Dit verschil was niet helemaal te verklaren, maar door deze ontdekking misschien wel. De microbiologen geven aan dat het kan komen doordat tetracycline zich niet tegen één, maar twee belangrijke processen in bacteriën blijkt te richten. Dit benadrukt de potentie van antibiotica die meerdere doelen kunnen raken. Verder blijken antibiotica die het membraan van bacteriën verstoren vaak effectiever te zijn tegen hardnekkige resistente bacteriestammen. Wenzel en collega’s stellen daarom dat met deze kennis tetracyclines ontwikkeld kunnen worden met verbeterde effecten tegen het membraan, in de hoop hierbij een bijdrage te leveren aan de strijd tegen multiresistente bacteriën.
Publicatie
Het onderzoek is open access gepubliceerd in het wetenschappelijk tijdschrift Communications Biology. Het volledige artikel is te lezen via deze link.